李俊杰医生的科普号
- 精选 乳腺癌保乳手术3
保乳手术切口该如何设计保乳手术原发灶的术式最常用的是肿瘤广泛切除(Lumpectomy),该术式在美国被广泛采用;另一种术式称为象限切除(Quadrantectomy),需要切除肿瘤所在部位的区段乳腺组织、表面覆盖的皮肤、下方的胸肌筋膜。在临床实际操作中,可以灵活选择上述两种手术方式,最为重要的是保证切缘阴性前提下确保外形的美观。 一般肿瘤位于乳房上方时,通常采用弧形切口切除肿块,外形较好和美观。当然有时肿块位于乳房腋窝尾部或者外上时也可以采用放射状切口,并向腋窝延伸,以便腋窝淋巴结可以整块切除。而位于乳房下方的病灶,则可采用放射状切口。伴随着肿瘤整复技术的运用,当前乳腺癌保乳手术的切口选择不止局限于放射性或弧形切口,位于不同象限的肿瘤可以采用双环切口、菱形切口、蝙蝠翼切口、类似于缩乳成行术的切口以及各种个体化的手术切口,通过肿瘤整复技术可以更方便的切除较多肿瘤周围的乳腺组织,并通过转移临近的脂肪及乳腺组织予以填充,并适当调整乳头的位置,从而在保证外观的情况下提高切缘阴性率,降低因切缘阳性而再次手术的风险。为使局部有较好的外形,目前并不建议做广泛的皮肤切除,如果肿瘤与皮肤无粘连,一般可保留肿瘤表面的皮肤,或仅做肿瘤表面一小片皮肤的切除,皮肤下可保留部分脂肪。但为了美观,有时可以切除和所需切除腺体量对应的皮肤,保证缝合后,外形比较饱满,没有明显的残腔。在手术操作中,切除的乳腺标本后必须及时进行切缘标记和,及时送病理检测,明确边缘、表面、基地是否有癌细胞累及。通常外科医师可以用缝线明确不同切缘,送检病理检测。并在切缘处放置钛夹标记,指引后续放疗。 肿块较大时,能否先化疗将肿块缩小再行保乳?伴随着综合治疗策略的进展以及患者对外形美观需求的增加,临床中将会遇见越来越多的患者,希望借助新辅助治疗以获得保留乳房手术的机会。早期的临床试验即发现,对不能保留乳房的患者,通过新辅助治疗,可提高保乳率。例如NSABP B18试验,新辅助化疗组的患者总体有效率为80%,其中将近1/2的患者获得临床完全缓解(cCR),使保留乳房治疗提高至68%,差异有统计学意义,特别是那些开始肿瘤>5 cm的患者,行新辅助化疗的患者有22%的可行保留乳房治疗,而先行手术的患者保留乳房治疗仅占8%。这些数据极大地增加了临床医师对新辅助治疗的信心,伴随着精准治疗理念的推广,个体化的新辅助治疗对局部晚期乳腺癌有了越来越高的缓解率,病理缓解率的增加也必然促使更多临床医师对于肿块较大而不可直接实施保乳手术的乳腺癌患者推行新辅助治疗。鉴于三阴性和HER-2阳性乳腺癌患者对新辅助治疗非常敏感,肿瘤退缩率更高,临床上对这些亚群的乳腺癌患者更可以高选择性的予以新辅助治疗,从而极大程度的地增加新辅助治疗后的保乳手术率。 如果患者拟在新辅助治疗后拟实施保留乳房手术,在新辅助治疗前建议进行完整的影像学评估,包括乳腺超声、钼靶、乳腺MRI基线评估乳腺和腋窝病灶的大小、范围等,并推荐在乳腺原发灶中心放置金属标志物,体表进行纹身标注肿块范围。新辅助治疗中,建议每2周期进行一次乳腺超声和(或)MRI检查,判定病灶的缓解情况。在具体手术操作前,需要注意的是新辅助治疗后肿瘤细胞的退缩有两种模式,一种为向心性退缩,肿瘤向心性缩小,形成较原来肿块体积小的瘤灶,此时肿瘤大小据实测量;另一种为非向心性退缩,即肿瘤退缩呈散在多灶,大体上肿块的大小可能与新辅助治疗前没有明显差别或较前缩小,但其中肿瘤细胞的密度发生了明显变化。因此向心性退缩的患者更容易在随后的保乳手术中取得成功,而非向心性退缩的患者,则有必要根据新辅助前标记的原发肿瘤范围进行完整的切除,以评估切缘是否阴性。 中国患者是否接受保乳手术?为了紧跟国外乳腺外科的发展趋势,我院早在90年代就已经开展乳腺癌保乳手术,并在上海乃至全国推广这种规范化的手术治疗策略,即保证疗效的最小最有效外科治疗模式。然而当前我国保乳治疗率相对较低,来自上海、北京等乳腺中心的回顾性研究显示我国保乳率约为5%-~20%,在主要的大型临床研究中心可能相对较高,在农村地区可能还不足5%。分析我国保乳率较低的原因可能包括:(1)由于我们缺乏基于群体的乳腺癌钼靶筛查项目,人群的防癌症意识较薄弱,大多都是患者自己触及肿块后进行就诊,由此患者确诊时肿瘤体积偏大,而乳腺体积又较欧美妇女较小,因此适合保乳患者的比例相对较低;(2)患者或医师担心保乳后的局部复发,加之中国社会整体的思维模式,患者“谈癌色变”,在诊断为乳腺癌后潜意识的地认为完整的切除乳房就等同于根治了肿瘤;(3)外科医师缺乏病理科的支持,由于保乳治疗中病理科医师承担着更为繁重的病理诊断工作,在医疗人力相对欠缺、医疗技术相对落后的情况下难以为全国所有地区患者提供准确病理评估的保证,从而限制了保乳治疗的实施;(4)缺乏保乳所需的放疗设施和经费,保乳手术和随后的放疗共同构成了一个完善的保乳治疗策略,而在我国绝大多数地区放疗设备的落后和欠缺,即便在大城市或医疗机构拥有较好的放疗设备也难以满足过多数量放疗的需求,加之放疗费用给患者带来的经济负担也不同程度的限制的保乳治疗的发展;(5)紧张的医患关系等等。因此需要加强医师对保留乳房治疗的认识,提高国内医师和患者对保乳的信心,通过我们共同努力来提高我国患者的保乳率和保乳成功率,让更多的乳腺癌患者在保证治疗效果的基础上进一步改善生活质量。 本文系李俊杰医生授权好大夫在线(www.haodf.com)发布,未经授权请勿转载。
李俊杰 副主任医师 复旦大学附属肿瘤医院 乳腺外科4702人已读 - 精选 乳腺癌内分泌治疗3
内分泌治疗的安全性和依从性这么多有效的内分泌治疗药物被研制出来,我们做出临床试验数据也证明非常有效,但现实的使用情况究竟如何呢?要知道那些有效降低风险的漂亮曲线一定是在坚持规范用药的前提下才可能实现。记得06年时我曾经做过一个我院病人的用药情况调查,通过逐一电话随访,发现3年以后仍然规范用药的比例不超过50%,而国外文献发显示,即便是临床试验的患者,在有专科科研医护团队督促,并免费赠药的情况下,患者5年的规范用药比例也只有81%。那么原因何在? 内分泌药物的毒副作用源自一项高危人群三苯氧胺预防试验的结果,比较了正常女性服用三苯氧胺和安慰剂的毒副作用。之所以用正常女性是希望能更客观真实的反应药物副作用水平。从两种人群各种细项副作用对比我们可以发现,安慰剂组反应出来的毒副作用比例(括号中的数据为占比)和三苯氧胺组居然是相似的,虽然在血栓和妇科疾病上确实略有增加,但总的来说差异不大。那您一定会问了,为什么和我们听说的,或者是和我切身感受差异如此之大?这里面我想有可能是心理上的归因问题导致的,因为随着年纪的增长,身体发生各种疾病的概率本就在增加,未见得真的是服用药物导致的,但因为有在吃药,所以很容易本能的就归咎到药物副作用上来。因此不仅是三苯氧胺,我们在芳香化酶抑制毒副作用的临床对比试验数据上也显示出相同的情况。 因此,临床上这种因为对毒副作用的妖魔化认知成为患者坚持长期规范用药的最大阻碍!所以,我希望我们广大患者朋友一旦出现了身体上的症状,可以和你的医生进行沟通,让医生帮你判断是否确实是药物引起的副作用,需要如何进行处理,千万不要擅自停药。 药物依从性影响治疗疗效刚才我有提到我们肿瘤医院06年左右用药的”依从性”大约在50%,而国外临床试验大约在80%,那么没有完成既定的治疗究竟危害有多大呢?下图是15年刚刚公布的新西兰的一份文献,它跟踪随访了两个城市5年的内分泌治疗情况,数据显示只有60%的患者有坚持规范服药,要知道这是一个有着非常好的高福利政策国家,”依从性“竟然也如此不乐观,由此可想我国现在的情况。 那么不按规范服药究竟危害有多大呢?研究数据显示,内分泌治疗服药量小于80%(相当于服药五天漏吃一天),复发风险增加2倍,而如果内分泌治疗周期小于1年,则死亡风险增加8倍!所以肿瘤本身不可怕,可怕的是不能坚持规范治疗!它就像高血压这类慢性病,只要能坚持长期规范用药,就能有很好的控制效果。 因为药物都有它自身的药效周期,一段时间过去,药物就会从身体中代谢出去,因此需要我们持续不断的进行用药,维持体内的药物浓度,身体才能至于药物的保护之下,因此三苯氧胺要求早一粒晚一粒,一定不要图省事,一次两粒;其他药物每天一粒,千万不要想起来才吃一粒,老是搞忘了。 哪些原因会影响药物依从性那么究竟有哪些具体原因影响到我们患者的”依从性“呢?16年一个问卷调查显示,以下几个原因被患者主要提及:疼痛/骨痛、潮热、情绪是三大主要原因。当然还有我们中国特色就是就医困难。下面我们就这三大主要原因一一进行讲解。 疼痛/骨痛 研究数据显示,使用AI进行内分泌治疗的患者较三苯氧胺会有更厉害的骨丢失速度,如果绝经前患者配合使用了卵巢功能抑制剂,或者是因为化疗导致卵巢功能早衰,则情况更为严重,因此骨折风险大大增加。研究显示AI治疗,骨密度降低风险概率显著增高,如果不进行干预,骨折发生率可能达到17%,因此,日常补钙和定期的骨密度监测是有必要的,适时的二膦酸盐(唑来膦酸)类药物的使用能有效改善骨质酥松风险。那么什么时候二膦酸盐必须使用呢,我们做骨密度检测会有一个T值,如果T值小于-2.0,这是个一个比较严重的骨折风险值,就必须使用。但由于我们的AI治疗会导致骨质流失的进行性加重,因此我个人认为在出现骨质低于正常值,比如T小于-1.0后就开始介入治疗是有意义的。而另一个让我给大家推荐二膦酸盐的原因是,前期临床实验数据显示,对早期患者来说AI治疗伴随3年的半年一次的二膦酸盐使用,可能进一步改善预后,至少不会更糟,因此我个人认为预防性使用是有意义的。 另外关于钙片的选择也是大家比较关心的问题,这里顺便提一下。其实钙片不是处方药,只要是正规厂家的都可以,医院开具的,药房购买的都行,不必过于纠结品牌。 血脂 很多时候我们会让患者在开始服用内分泌治疗药物的第1或第3个月检测血脂情况,如果血脂有问题,会建议患者去内科进行抗血脂治疗。这是因为血脂不单单和肿瘤相关,还和我们很多的基础疾病,比如心梗、脑梗等相关联。由于现在大家吃得越来越好,这方面出现问题的概率大大增加,这个时候如果再因为我们的内分泌药物导致肝功能损伤,进而代谢能力下降,增加血黏度,将来出现心梗、脑梗的风险就会增大。 下图是来自美国SEER数据库63566例乳腺癌患者的死亡原因调查,研究发现随着时间的推移,10年以后,患者死于乳腺癌本身的原来越少,最后心脑血管疾病(CVD)因素反倒超越乳腺癌成为死亡的首要原因,达到了15.9%。因此,在我们的抗肿瘤治疗过程中,对这些基础性疾病因素的提前预防就显得尤为关键。发现问题,及时的药物干预,或者药物更换,就能够更好的预防此类风险的发生。 心理健康 这个因素在目前国内还不太被关注到,但我每次都会重点和患者朋友们讲下这个问题。在全世界,尤其是欧美比较好的诊疗中心,都会配备有一个科室专门负责和肿瘤患者进行心理疏导、沟通,告诉你如何才能身心健康,如何运动,如何保持体重。它们做过很多研究,包括如果一个乳腺癌患者,在治疗之后,如果能每周能保持运动达到150分钟(相当于每周五天,平均每天半个小时),比那些达不到此标准的患者,能显著改善预后,当然,研究也发现更长时间的运动并不能进一步获益,因此运动适量即可。另外,内分泌治疗药物可能一定程度上带来抑郁,与专业医护人员的沟通疏导,能一定程度上降低患者的抑郁程度,而适当的运动也有助于缓解焦虑、抑郁。而且,我们乳腺癌的致病因非常复杂,遗传其实只占非常小的比例,大多都是环境因素影响,虽然也有外部大环境,但那个我们无力改变,而内部的心理环境、情绪压力更为关键。因此保持良好的运动习惯、积极的心态,能够让大家更好的面对治疗中的副作用,帮助大家更好的战胜疾病! 今天讲了这么多,总的来说就是希望大家增强大家的信心,明白我们内分泌治疗的机制原理,从而能够正确、理性、积极面对我们治疗过程中可能产生的种种问题,增加依从性,争取彻底治愈我们的疾病,赶走肿瘤君!最后祝大家健康!谢谢大家!
 李俊杰 副主任医师 复旦大学附属肿瘤医院 乳腺外科3337人已读
李俊杰 副主任医师 复旦大学附属肿瘤医院 乳腺外科3337人已读 - 精选 乳腺癌内分泌治疗2
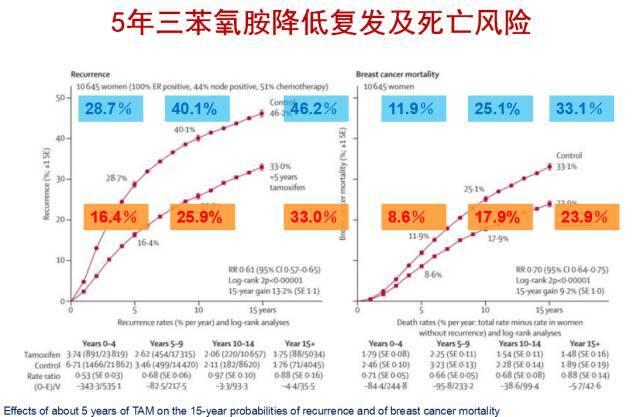
常用内分泌治疗药物三苯氧胺(早一粒晚一粒) 三苯氧胺是内分泌治疗中疗效非常好的经典用药,虽然它一个月只要二十几块钱,但千万不要小看它,便宜只是因为它研制出来已经有三十多年了,工艺成熟,而且被国产化。目前所有内分泌药物的临床试验都必须拿三苯氧胺作为参照对比,只有疗效明显好于三苯氧胺才会被批准临床使用。 从下图数据大家可以清楚的看到,左图是我们追踪激素受体阳性患者术后15年的复发转移曲线,上面一条线是不使用三苯氧胺,下面一条是使用了5年的三苯氧胺,我们可以清楚的看到,从第五年开始,两条曲线间始终保持了10%以上的差异率,也就是说,三苯氧胺可以将我们的复发转移风险降低至少10个以上的百分点。在右图的死亡率上也显示出同样的差异。这还是在治疗手段相对缺乏的年代产生的数据。 而且5年三苯氧胺的获益还具有延期效果,我们从曲线走势就能看出,服药5年停药后,两条曲线并未出现收窄现象,而是一直维持差距到15年,因此我们说5年的三苯氧胺使用可能将帮助你获得下一个五年的生存获益。 卵巢功能抑制剂(每月一次/三个月一次,皮下注射) 研究发现,卵巢分泌雌激素其实是由大脑下丘体释放出一种叫促性腺激素释放激素(GnRH)的物质,当我们的脑垂体接收到GnRH后就会向血液中释放出黄体生成激素(LH)、促卵泡成熟激素(FSH)这两种物质,当卵巢接收到这两种信号后,就会开始分泌雌激素。因此诺雷得/抑那通的药物机理就是通过模拟GnRH,让脑垂体的对应受体接收到假的信号,从而停止LH和FSH这两个信号的发出,让卵巢处于一种暂时的休眠状态,从而实现女性血清中雌激素水平的下降。 但当你首次用药的前7-10天,由于体内原本有GnRH,进入体内的GnRHa会让脑垂体识辨不清,会引起激素水平应激性升高,因此我们一般会要求患者在注射后10-14天左右,体内激素水平趋于低位稳定后再开始化疗。 卵巢抑制和生育的关系是年轻乳腺癌患者一直以来都非常关注的话题。我们知道化疗会对卵巢带来不可逆的损伤,化疗期间让卵巢功能暂停可能帮助我们一定程度上减轻伤害。对于那些需要进行内分泌治疗的年轻患者来说,何时进行生育是一个最优选择,目前在医学界仍然是一个研究中的议题。目前有一个专项的临床试验正在欧美进行,实验设计是,在内分泌治疗2-3年后全部停药,给予3个月的卵巢恢复时间,再给予2年的受孕时间,2年窗口期结束,无论受孕与否都将停止,重新恢复内分泌治疗。目前该实验已经开展1年多,在今年8月第一例宝宝已经成功来到世界上,对于这个实验的后续进展我们将一直保持关注。因此,对于我们年轻的乳腺癌患者,术后生育是完全可能的,特别是复发风险比较低的患者,但一定要在专科医生的指导下进行,需要患者、家属、专科医生甚至是妇产科医生的共同参与配合,千万不能自己想当然,说听了今天的讲座,服药两年就擅自停药进行受孕。 芳香化酶抑制剂(AI每天一粒) 目前常用的芳香化酶抑制有三种:依西美坦、来曲唑、阿那曲唑,临床中经常被患者问道那种药最好?是国产的好还是进口的好?其实大家要知道,如果说其中某种药效果会明显好于其余两种,另外两种药是不会有市场的。这三种药药理类似,临床上大量数据证明,其疗效不存在实质性差异,无论是国产药还是进口药,在疗效上也大致相似。如何选择完全根据医保和个人的经济状况。但有一点更为重要,那就是药物毒副作用耐受性的问题,只有服药后耐受性好,你才可能长期坚持用药。临床上我们确实发现,虽然三种药物毒副作用差异不大,但有的患者就是对某种药不耐受,换药后就能获得好转,而且这种更换并无规律,A换B,B换C,C换A,国产换进口,进口换国产,都有可能,因此在没有出现耐药的情况下,只有毒副作用,只有身体耐受情况,是你是否需要换药的重要原因。 那么为什么对于绝经后女性我们会采用芳香化酶抑制(AI)呢?因为研究数据显示,五年的AI相对于三苯氧胺着更好的效果,5年的复发风险从12.5%下降至9.7%,9-10年的风险值从20%左右降至16%左右。虽然看似指数下降得貌似不是特别高,只有几个百分点,其实这里需要说明的是,这是和已经有着显著效果的三苯氧胺相比,是三苯氧胺之上的进一步获益。其道理就是,对于绝经前女性来说,体内充盈着大量的雌激素,三苯氧胺作为雌激素受体抗拮剂,它有着大量的目标明确竞争对手,针对性强;而对于绝经后女性而言,体内雌激素水平相对比较低,这个时候我们去针对性的控制外源性雌激素转化通路,釜底抽薪,就能有更好的效果。 对于AI的使用有一点是非常关键的,那就是——判断是否绝经。因为AI一定是针对绝经后女性才可以使用的,否则整个治疗策略就是错误的。临床上经常碰到患者因为停经一段时间就会来询问是否可以换药。由于化疗会对卵巢造成一定伤害,可能造成绝经时间提前,但也有可能只是月经紊乱或治疗后暂时闭经。因此,虽然中国目前妇女的平均绝经年龄是52岁,但由于个体差异,年龄并不能成为判断是否绝经的标准。临床上我们对绝经的定义是卵巢合成雌激素功能永久丧失,生理性的月经永久终止,因此在“中国绝经前女性乳腺癌患者辅助治疗后绝经判断标准及芳香化酶抑制剂临床应用共识”中“永久性停经(绝经)“的判断标准为:1、年龄≧50周岁,化疗后或在服用SERM(三苯氧胺/法乐通)药物期间闭经至少12个月,且E2(雌二醇)、FSH(促卵泡生成素)连续测定至少3次均达绝经后水平者;2、年龄在45—55周岁,化疗后或在服用SERM药物期间闭经至少24个月,且E2及FSH水平连续测定至少3次均达到绝经后水平者;3、年龄
 李俊杰 副主任医师 复旦大学附属肿瘤医院 乳腺外科2690人已读
李俊杰 副主任医师 复旦大学附属肿瘤医院 乳腺外科2690人已读 - 精选 乳腺癌内分泌治疗1
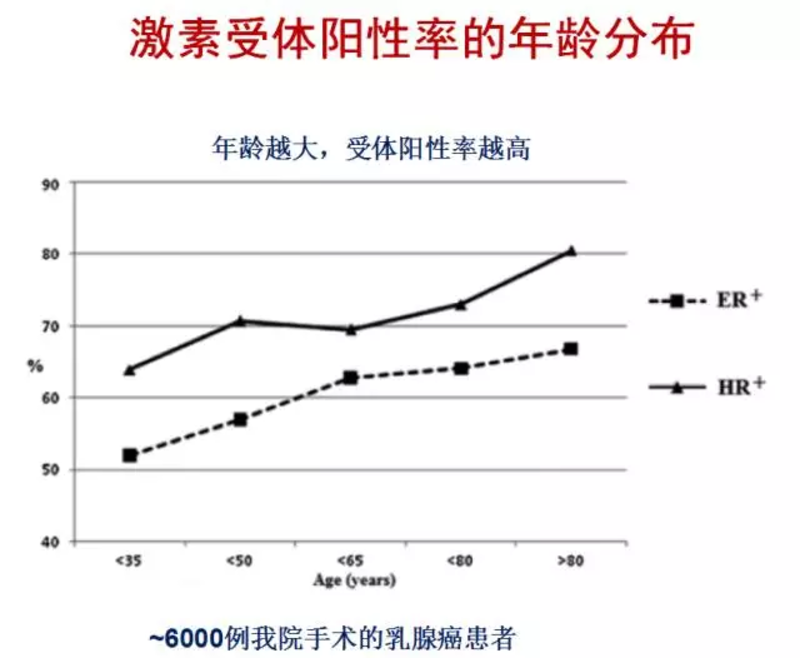
我们的主题是内分泌治疗,那为什么要进行内分泌治疗?你可能会说,因为我是激素受体(ER/PR)阳性。不全对!并不是所有激素受体阳性患者都需要内分泌治疗,之所以要求进行内分泌治疗,是因为你有复发转移风险。比如非常早期的导管原位癌的患者,进行了全乳切除后,即便她激素受体是阳性,通常我们不会推荐她进行内分泌治疗,因为这种疾病复发转移风险很低。因此,无论淋巴结阳性或是阴性,肿块大或是小,它们只是预示的风险的高低程度不同。有时已经进行了长期的内分泌治疗,但医生仍要求继续进行内分泌治疗,其原因就在于医生认为可能其仍然具有较高的复发转移风险。 下图数据是多年前,我的一篇论文中总结分析的结论,我统计了我院7000多例乳腺癌患者年龄和激素受体情况,发现患者随着年龄增长,激素受体阳性占比出现逐渐增高的趋势,80岁群体中激素受体阳性患者占比可达65-%-80%,而小于35岁患者占比大约只有一半。 内分泌治疗策略什么是ER?ER是指雌激素受体,不是雌激素,很多患者对这两个概念容易混淆,这里用这张图(图4)简要给大家解释下。图中这个大圆圈是我们的细胞,里面那个小圆圈是细胞核,那个红色的E代表雌激素,雌激素要想进到细胞核中发生作用就需要ER这个雌激素受体进行装载,把它带进去,这样细胞核才能进行增长、生殖、发育、分裂。 雌激素消除模式 也就是从源头上抑制雌激素的产生,例如我们绝经前患者进行卵巢功能抑制,也叫卵巢去势,目前有手术、放疗、药物三种方法,由于药物抑制相对损伤较小、作用可逆,因此现在临床上更多推荐药物去势,代表药物为诺雷德和抑那通。从疗效上它们没有区别,只不过对于乳腺癌患者,诺雷德采用的是一个月的剂型进行的临床试验,而抑那通是三个月的剂型;对于绝经后患者,虽然卵巢已经停止了工作,但身体仍然会通过外源性物质转化为雌激素,而这个转化过程需要一种叫芳香化酶的物质参与帮助,因此对于绝经后患者可以通过服用芳香化酶抑制剂来达到降低体内雌激素的水平,目前主要使用的有依西美坦、来曲唑、阿那曲唑三种,它们在疗效上也非常相似。 通路干扰模式 也就是干扰ER的正常工作,让药物伪装成一个假的雌激素,从而使细胞核接收不到上游的信号,也无法进行生殖分裂,进而走向凋亡。三苯氧胺(它莫昔芬)和法乐通(托瑞米芬)就是这样一类药物,它拥有和雌激素类似的分子结构,通过每天持续不断的服药,竞争性的结合细胞内的ER,从而对其形成抑制。现在还有一种更新的药物叫氟维司群,它不仅迷惑ER,同时还会破坏、降解ER,目前已批准用于一些晚期患者。
 李俊杰 副主任医师 复旦大学附属肿瘤医院 乳腺外科3676人已读
李俊杰 副主任医师 复旦大学附属肿瘤医院 乳腺外科3676人已读 - 精选 乳腺癌预后的不断改善
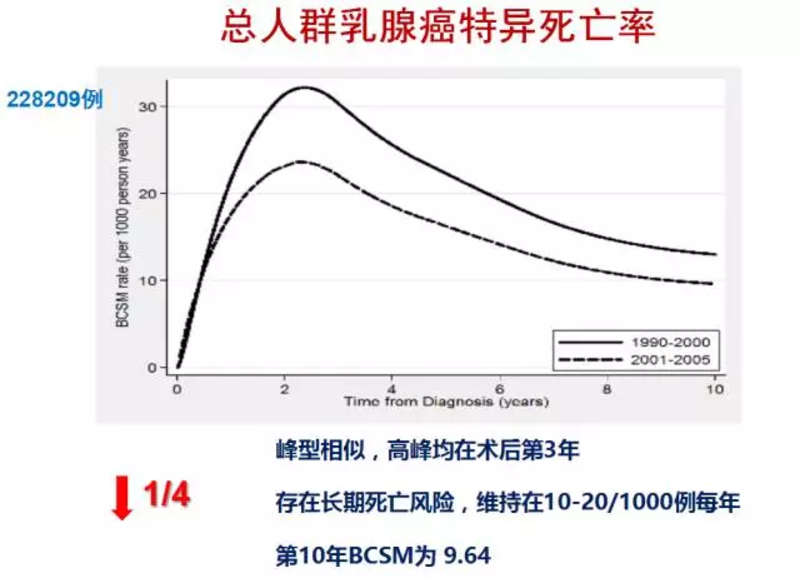
随着医学进步,乳腺癌治愈率不断提升,总体乐观下图是我刚发表的一篇论文里的数据,我总结了22万美国乳腺癌患者在90年代初和进入20世纪以来,跟踪十年生存率对比。从20世纪以后的这条虚线曲线我们可以看出,乳腺癌在2-3年出现一个峰值(2%左右的死亡率)后,随着时间的推进,会逐渐下降到5年以后的每年1%左右,也就是说我们乳腺癌累计十年的总生存率可以达到85%以上,是一个非常乐观的预后。其次,通过对比90年代和2000年以后这两条曲线,我们可以发现,他们形态完全一致,也就是说,通过新的治疗手段的使用,通过我们更加科学有效的综合治疗(化疗、内分泌治疗、靶向治疗等等),治愈率上获得了整体提升,而不只是推迟疾病的复发转移或死亡时间,否则在波形上应该会出现延迟。因此,我希望大家一定要有信心,一定要积极配合我们完成既定的治疗方案,因为新的治疗策略意味着治愈更多的患者。如果期间有任何的毒副作用状况产生,也不必过于担心,立刻来找医生,我们会给予相应的辅助药物帮你解决问题,让你将治疗顺利推进下去。 不同分子分型复发转移风险特性不同,无所谓好坏,不具可比性至于究竟是激素受体阴性好还是阳性好?从下图(图左为激素受体阴性、图右为基数受体阳性)我们可以看出,这两种不同类型的乳腺癌复发转移风险有着明显不同,如图所示,激素受体阴性患者的死亡风险主要集中在前5年,后面会急剧下降,因此如果你是一个三阴患者,现在已经平安度过5年,那么可以恭喜你,极大概率是治愈的;但反观这些激素受体阳性的患者,虽然总体复发转移风险不高,前5年最高峰值也就在1.5%左右,但随着时间的推移,风险值却保持平稳,并不会进一步下降,因此这也就是我们内分泌治疗一定需要长期坚持的道理所在。 乳腺癌现代标准化规范治疗手段持续降低复发转移率乳腺癌标准治疗手段主要包括:手术治疗、化疗、放疗、靶向治疗和内分泌治疗五种。近期一篇论文的研究数据揭示这五种治疗手段分别对乳腺癌预后起到的作用。1950年以前,乳腺癌的有效治疗基本只有手术,通过手术相对于不治疗能降低50%左右的死亡风险,到上世纪7、80年代,出现了化疗、放疗、内分泌治疗,到近十年的靶向治疗手段,它们不断的在预后上做加法,数据显示,分别能进一步降低10%、8.5%、10%和6.4%的复发转移风险,使得我们现在乳腺癌的总体生存率提升到85%左右的水平,并且现在仍然在不断的提升中。在这里从数字中我们可以看出内分泌治疗的效果非常显著,其必要性也不言而喻。
 李俊杰 副主任医师 复旦大学附属肿瘤医院 乳腺外科2490人已读
李俊杰 副主任医师 复旦大学附属肿瘤医院 乳腺外科2490人已读 - 医学科普 乳腺癌保乳手术2
保乳手术的切缘问题保乳手术的实施需同时保证切缘阴性以及外形的美观,这是一个相对矛盾的命题。理论上来说切除肿瘤及周边正常乳腺组织越多,越容易得到一个阴性的切缘,从而可以降低再次手术率和术后局部复发的风险,但切除越多的组织也必然对术后乳腺外形的美观带来更大的挑战。因此最完美的方式是,在保证切缘阴性的情况下尽可能减少正常乳腺组织的切除率,这就需要临床外科医师术前进行仔细的临床体检、认真参阅影像学检查结果后设计手术路径和方案,并和病理科医师进行密切的合作以判断是否完整的切除了病灶。在手术中,对切除标本各切缘进行定向标记,不仅有利于病理检查,而且在某一侧切缘阳性时,可以避免再次切除原手术残腔周围大量正常组织。我们有必要了解保乳手术切缘阴性的具体定义,以及常用的病理评估切缘的方法。 1) 切缘阴性的定义。 自保乳手术开展至今,临床中对于安全阴性切缘的定义不断的在发展和完善。肿瘤的切缘宽带,指肿瘤边界距离切除组织表面的距离。早期研究报道,在保乳病例中如果切除肿瘤周围0.5-~1.0cm的正常组织,那么95%的病例手术切缘组织学检查为阴性。随后有文献指出,虽然切缘阳性意味着更高的局部复发率,然而在切缘阴性的患者中,切缘宽度的大小和局部复发率之间并无显著关联,因此后续的临床研究不断尝试着将安全切缘的宽度从1cm降到1mm甚至更小的可行性和安全性。近期越来越多的数据推荐采用墨汁染色评估切缘,并规定切缘无肿瘤(no ink on any cancer cells)即可确认为切缘阴性。只要保证切缘阴性即可,扩大切缘(>1mm,>3mm,>5mm等)均不会进一步降低同侧乳腺复发率。当然也有新的研究提示2mm以上的切缘有着更好的局部控制率,但绝大多数的指南均将切缘阴性定义为墨汁染色切缘无肿瘤,也提示我们日常工作中切忌没有必要盲目的扩大切缘,即没有获得更好的疗效,同时又影响术后美观。 2) 切缘的评估方法 肿物边缘法和残腔边缘法是两种最为常见的评估保乳切缘的病理方法:肿物边缘法和残腔边缘法。肿物边缘法首先在NSABP B06试验中提出和采用,将广泛切取的肿瘤标本不同切面采用不同颜色的墨汁进行染色,随后再进行石蜡固定,并在最终的石蜡病理组织中通过染色判断肿瘤和墨汁染色切缘的位置距离确定保乳手术具体的切缘,国际上广泛采用该方法予以病理切缘的评估,更为的准确但相对耗时耗力,前文中提出的墨汁染色无肿瘤作为切缘阴性的定义也来自于这种病理评估的方法;第二种是残腔边缘法,即广泛切取标本后,在残腔周围的不同方位再补充切除一定的腺体进行病理切缘的评估,该方法切除组织较少,工作量也降低。 目前全球乳腺癌绝大多数指南都推荐采用肿物边缘法,并对标本进行垂直切缘放射状取材,以便在固定后的石蜡标本中,镜下观察时能对切缘作出准确定位,并正确测量肿瘤和切缘的距离。但目前在国内主要采用的保乳切缘病理诊断方法仍为残腔边缘法,通过不同切面方向上再次切去少量乳腺组织进行冰冻病理送检,可以在手术操作中得知切缘情况,从而假设切缘阳性即刻可进行再次手术予以评估。
李俊杰 副主任医师 复旦大学附属肿瘤医院 乳腺外科2963人已读 - 医学科普 乳腺癌保乳手术1
保乳手术的预后和手术指证保乳手术的问世已经30余年了,其目标是通过保乳手术及放疗使乳腺癌患者达到与根治性手术相同的生存率,同时要求患侧乳房复发率低,并且有良好的美容效果。早期多项大样本的临床随机试验均把乳腺癌保乳治疗与根治性手术进行比较,均发现两种治疗方法生存率相似,譬如EORTC 10801研究对968例患者经过长达22.1年的随访,发现保乳术和全乳切除术在总生存和无远处转移生存上差异无统计学意义差异。保乳治疗可以取得很高的局部控制率及令人鼓舞的美容效果,长期的随访有助于人们了解保乳治疗后局部复发的方式、病程,局部复发相关的因素及影响乳房外形的因素。近期一项回顾性研究对T1-2N0-1M0原发性乳腺癌患者经过11.3年的随访发现,保乳患者的总生存更好、有更低的远处转移率和区域复发率。这些结果为明确保乳手术、放疗的方式、及保乳治疗指征提供了有效的依据,保乳手术联合全乳放疗的疗效等同于全乳切除手术,对合适的患者给予保乳治疗是安全有效的 。 随着人们群癌症防范意识的不断增强、钼靶筛查的普及以及影像技术的提高,越来越多的乳腺癌得以被早期诊断,因此保乳治疗的实施率越来越高,在欧美发达国家60%~70%的早期乳腺癌患者接受了保留乳房的手术。然而我国保乳率还相对较低,鉴于早期多项研究均证实了保留乳房手术联合后续放疗的生存率等同于或至少不低于全乳切除手术,因此我们需要正视保留乳房手术的安全性,切不可盲目选择不必要的全乳切除或预防性乳腺切除手术,造成过度治疗。在精准医学时代,我们也有理由提出“选择合适的早期乳腺癌患者给予保乳治疗是安全可行并推荐的治疗策略”的口号。 保乳手术的指证 在我国开展保留乳房手术,通常建议参考由中国抗癌协会乳腺癌专业委员会编写的《中国抗癌协会乳腺癌诊治指南与规范》(以下简称《指南与规范》)。2017版的《指南与规范》第7章,对“浸润性乳腺癌保乳治疗临床指南”进行了详细的谈论和规范,一方面保留了谨慎的态度,对保乳乳房手术的实施进行了详细的适应证和禁忌证的规定;同时也鼓励所有符合保乳适应证的患者,更多的接受该治疗模式。 保乳手术适应证: 主要针对具有保乳意愿且无保乳禁忌证的患者。肿瘤大小属于T1和T2分期;乳房有适当体积,肿瘤与乳房体积比例适当;术后能够保持良好的乳房外形的早期乳腺癌患者;对于多灶性乳腺癌(同一个象限的多个病灶,假定是来源于同一个肿瘤),也可以进行保乳手术;Ⅲ期患者(炎性乳腺癌除外) 经术前化疗或术前内分泌治疗降期后达到保乳手术标准时也可以慎重考虑。 保乳手术绝对禁忌证: (1) 妊娠期间放疗者。然而对于妊娠妇女,可以采取保乳手术可以在妊娠期完成进行保乳手术,放疗可以在分娩后再进行放疗。 (2)病变广泛或确认为多中心病灶,广泛或弥漫分布的恶性特征钙化灶,且难以达到切缘阴性或理想外形。 (3)肿瘤经局部广泛切除后切缘阳性,再次切除后仍不能保证病理切缘阴性者。 (4)患者拒绝行保留乳房手术。 (5)炎性乳腺癌。 保乳手术相对禁忌证: (1)活动性结缔组织病,尤其硬皮病和系统性红斑狼疮或胶原血管疾病者,对放疗耐受性差。 (2)同侧乳房既往接受过乳腺或胸壁放疗者,需获知放疗剂量及放疗野范围。 (3)肿瘤直径大于5 cm者。 (4)侵犯乳头(如乳头Paget病)。 (5)影像学提示多中心病灶(多中心病灶指在2个或2个以上象限存在1个及以上病灶,或病理类型和分子分型完全不一样的两个乳腺病灶)。 (6)已知乳腺癌遗传易感性强(如BRCA1/2突变),保乳后同侧乳房复发风险增加的患者。
李俊杰 副主任医师 复旦大学附属肿瘤医院 乳腺外科1743人已读 - 医学科普 乳腺癌手术治疗的历史、现状和发展
1 物理学的根治 现有的乳腺癌治疗模式是从曾经单纯的手术切除模式慢慢演变、发展而来的。根据医史记载,乳腺癌的局部治疗起始于公元前3000年至公元前2500年的古埃及,残酷的烧烙用于治疗许多乳腺疾病。直至文艺复兴时期,以安德雷亚斯·维萨里(Andreas Vesalius,1514~1564)为代表,引领解剖学的创立,使乳房切除从野蛮的烧烙走向以血管结扎为基础的解剖外科时代。 1757年法国手术学奠基人吉恩·路易斯·珀蒂特(Jean Louis Petit,1674~1750)提出将乳房、可触及的淋巴结、与肿瘤粘连的胸大肌作整块切除;1867年,英格兰的查尔斯·穆尔(Charles Moore,1821~1870)详细阐述了乳腺癌手术的基本原则,提倡肿瘤的广泛切除,并在20世纪被广泛接受。理查德·冯·福尔克曼(Richard von Volkmann,1830~1889,德国外科医师)于1875年建议在行全乳切除、腋窝清扫术的同时整块切除胸大肌筋膜;威廉·史都华·豪斯泰德(William Stewart Halsted,1852~1922,美国知名外科医师、近代外科学之父、约翰霍普金斯医院外科主任、四大创院教授)在前者提出的术式上加以发展,于1894年报道了根治手术治疗50例乳腺癌患者的经验,该手术切除全部乳房、胸大肌和腋淋巴结,其在1894、1898和1907年发表的论文使乳腺癌根治性全乳切除被广泛接受并影响了20世纪前3/4的时代。豪斯泰德时期,大多数乳腺癌患者属局部晚期,3/4的患者存在腋淋巴结转移;以往的手术治疗局部复发率达60%~82%,3年生存率为9%~39%,豪斯泰德报道的局部复发率为6%,3年生存率为38%~42%,10年生存率为12%。该手术以乳腺癌的局部播散,特别是淋巴道的播散为理论依据,由此只要进行乳腺癌所在区域的广泛切除术+引流淋巴结区域清扫术,就能达到根治的效果。因此乳腺癌根治术要求将患侧乳房、表面皮肤、胸肌和整个腋窝组织作整块切除。为了获得更好的疗效,随后还相继出现了清扫内乳淋巴结的乳腺癌扩大根治术、超根治术,甚至前1/4截肢术。 2 生物学的根治 人们慢慢发现盲目扩大手术切除的区域并不能进一步改善乳腺癌患者的预后。1948年,大卫·霍华德·帕蒂(David Howard Patey,1899~1977,英国外科医师)提出切除胸大肌并不能提高根治性全乳切除的手术疗效,他描述了一种改良的根治性全乳切除术,即切除乳房、胸小肌和腋窝内容物,保留胸大肌;休·奥欣克洛斯(Hugh Achincloss,1915~1998,美国外科医师)和约翰·马登(John Madden,美国外科医师)进一步改良了该术式,同时保留胸大肌和胸小肌。接着,许多大样本回顾性分析和两项前瞻临床研究证实,无论局部控制还是生存率,改良根治术与豪斯泰德根治术效果相当。因此,采用改良的根治性全乳切除术的比例自20世纪70年代初的27.7%不断上升,至1982年,改良根治术占全乳切除根治术的72.3%。20世纪70年代,伯纳德·费希尔(Bernard Fisher,1918~,美国外科医师,NSABP创始人之一)对此提供了理论依据,认为乳腺癌从发病开始就是全身性疾病,乳腺癌手术治疗失败往往是因为癌细胞早期的全身播散。人们充分认识到盲目扩大切除范围的手术并不能治愈乳腺癌,只会降低患者的生活质量。只有针对全身进行系统性综合治疗,才会进一步改善乳腺癌的预后,由此乳腺癌的综合治疗进入了高速发展阶段。外科治疗的模式也从“物理学的根治”逐步过渡到“生物学的根治”。基于费希尔新的理论所进行的NSABP B-04研究证实,腋淋巴结临床阴性的乳腺癌病例随机接受根治术、单纯乳房切除加腋窝放射治疗、单纯乳房切除和腋窝随访(有腋淋巴结转移时再行手术),3种治疗方式的长期生存率相似,这一结果有力地证实了费希尔理论,同时成为乳腺癌局部治疗发展史上的另一个里程碑,为当今乳腺外科的发展奠定了基础。 3 注重疗效和生活质量 最近40多年来,由于综合治疗手段的逐步被发掘、被证实,从根本上改变了乳腺癌的外科治疗理念,从曾经“最大可耐受”治疗模式逐步发展为目前的“最小最有效”治疗模式。其中特别值得关注的包括保乳手术、腋窝前哨淋巴结活组织检查术和乳房重建手术的普及和推广。 3.1 保乳手术 保乳手术已问世30余年,其目标是通过保乳手术和放射治疗使乳腺癌患者达到与根治手术相同的生存率,同时要求患侧乳房复发率低,并且有良好的美容效果。几项大样本的临床随机研究均把乳腺癌保乳治疗与根治手术进行比较,结果发现两种治疗方法的生存率相似,说明局部治疗方法的差异并不影响大多数乳腺癌患者的生存率。欧美许多医疗中心还进行了有关保乳手术的回顾性研究,不仅验证了保乳手术可以取得很高的局部控制率和令人鼓舞的美容效果,而且长期随访有助于了解保乳手术后局部复发的方式、病程、局部复发相关的因素和影响乳房外形的因素。这些结果为明确保乳手术、放射治疗的方式,以及保乳治疗指征提供了有效的依据。随着人们癌症防范意识的不断增强、钼靶筛查的普及和影像学技术的提高,越来越多的乳腺癌得到早期诊断,因此保乳手术的实施率越来越高,在欧美发达国家,60%~70%的早期乳腺癌患者接受保乳手术,不仅获得了相似的生存预后,还进一步改善了生活质量,该治疗模式已经成为当前早期乳腺癌的一种标准治疗模式。 3.2 腋窝前哨淋巴结活组织检查术 前哨淋巴结的概念基于一种假说,即原发肿瘤可通过淋巴管到达特定淋巴引流区域的第1个淋巴结,称为前哨淋巴结。通常有4种方法可判定乳腺癌患者腋窝前哨淋巴结的部位:①染料法;②术中核素法;③术前淋巴显像+术中核素法;④染料与核素联合法。通过示踪剂的指引,乳腺癌患者平均可以找到2~3枚腋窝前哨淋巴结。评估前哨淋巴结的病理学检查方法包括石蜡病理学检查或术中病理学检查,后者包括快速冰冻切片和印片细胞学等。目前淋巴结内存在1个以上最大径>2mm的肿瘤病灶定义为宏转移,肿瘤病灶最大径>0.2mm但≤2.0mm定义为微转移,而单个细胞或最大径≤0.2mm的小细胞簇为孤立肿瘤细胞。一系列乳腺癌前哨淋巴结活组织检查的大型前瞻随机临床研究,对于临床淋巴结阴性的早期乳腺癌患者实施前哨淋巴结活组织检查术,如为阴性,则部分患者不再行腋窝清扫术。长期随访提示,未行腋窝淋巴结清扫术的前哨淋巴结阴性患者的局部控制率和生存率等同于行腋窝淋巴结清扫术的患者,故对于乳腺癌早期患者而言,前哨淋巴结活组织检查术可以取代腋窝淋巴结清扫术。因此,目前对于临床腋窝淋巴结阴性的早期乳腺癌患者,腋窝前哨淋巴结活组织检查术已经成为标准的腋窝淋巴结处理方式,当前的研究热点在于:①前哨淋巴结微转移或1~2枚宏转移时,可否无需补充行腋窝淋巴结清扫术;②腋窝淋巴结阳性患者新辅助治疗降期后可否通过前哨淋巴结准确评估腋窝状态,从而使部分腋窝淋巴结转阴的患者免行腋窝淋巴结清扫术。 3.3 乳房重建手术 乳房重建手术旨在帮助乳腺癌患者重塑身体外形,使两侧乳房外形基本对称,能够使患者在穿衣后自信地恢复正常的社会和生活角色。按手术的时机主要分为即刻重建和延期重建。即刻乳房重建指在切除乳腺肿瘤的同时进行乳房整形,包括以下优点:①切除和重建一次完成,缩短住院时间和减少费用;②患者不会存在失去乳房的心理痛苦;③重建乳房的外形更好;④不推迟后续辅助治疗的时间,也不会增加局部复发的风险。即刻乳房重建通常适合于保留皮肤的乳房切除患者,手术留下了足够的乳房皮肤以供即时重建时使用,这些自体的皮肤具有最自然的外观和手感。延期乳房重建指在乳腺肿瘤切除并完成辅助治疗后再进行重建手术。常用的重建技术包括自体组织重建(带蒂肌皮瓣、游离肌皮瓣乳房重建)、假体重建(扩张器置换假体)和乳头重建技术等。任何乳房重建手术都不应该干扰乳腺癌的标准手术治疗和其他综合治疗。随着重建技术的发展和综合治疗的进步,当前对早期、生物学行为较好的乳腺癌患者还可开展保留乳头乳晕复合体联合即刻乳房重建术,以达到更好的术后外形;在保乳手术中也可运用容积移位或容积置换技术(自身脂肪填充)等肿瘤整形手术技术,以修复因广泛切除乳腺组织后导致的乳房局部凹陷、乳头移位、轮廓畸形等乳房外观的不满意。
李俊杰 副主任医师 复旦大学附属肿瘤医院 乳腺外科4504人已读





